科研 | 中国海大:虾青素通过调节肠道菌群减缓H22荷瘤小鼠在索拉菲尼治疗期间的骨骼肌萎缩
论文ID
实验设计
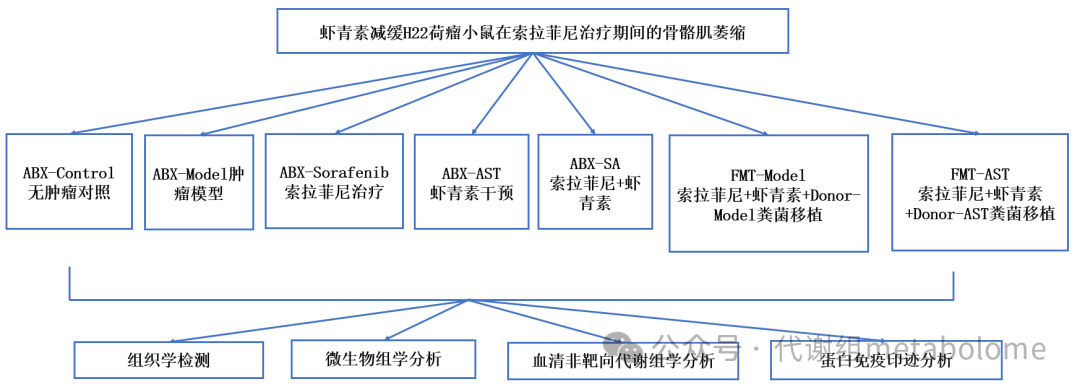
实验结果
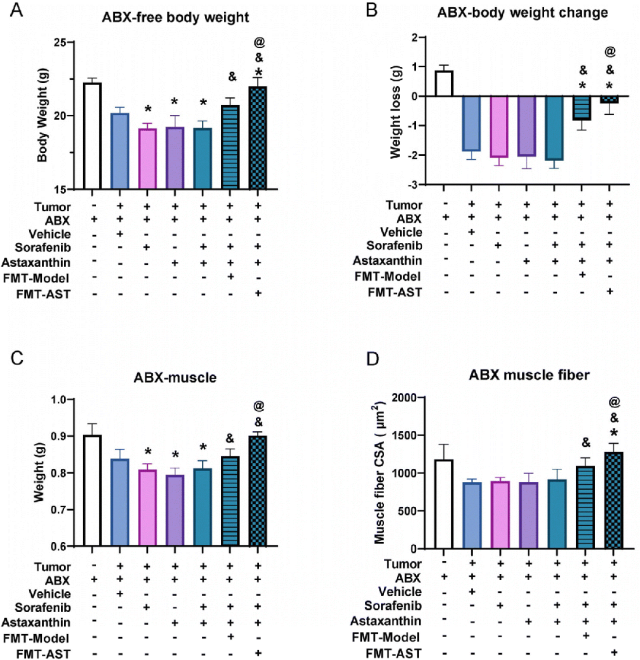
为了研究肠道菌群对虾青素缓解分子靶向治疗诱导的骨骼肌萎缩的潜在影响,作者给小鼠注射了广谱抗生素,以消除肠道菌群。索拉菲尼治疗导致伪无菌荷瘤小鼠的体重显著下降(图1A、B,P < 0.05)。然而,虾青素没有降低伪无菌荷瘤小鼠的体重(图1A、B)。骨骼肌萎缩是癌症相关恶病质中体重减轻的重要诱因之一。索拉菲尼治疗加剧了伪无菌荷瘤小鼠骨骼肌质量的下降,在这期间补充虾青素没有改变这一损失(图1C)。然而,在索拉菲尼结合虾青素治疗期间,粪菌移植可以有效缓解伪无菌荷瘤小鼠的体重减轻和骨骼肌萎缩(图1A-C,P < 0.05)。与FMT-Model组(索拉菲尼治疗期间膳食补充虾青素且进行Donor-Model小鼠的粪菌移植,Donor-Model为灌胃橄榄油的肿瘤小鼠)相比,FMT-AST组(索拉菲尼治疗期间膳食补充虾青素且进行Donor-AST小鼠的粪菌移植,Donor-AST为灌胃虾青素的肿瘤小鼠)效果更明显,且FMT-AST组小鼠的骨骼肌质量明显高于FMT-Model组(图1C,P < 0.05)。
骨骼肌纤维横截面积的分析证实,在索拉菲尼治疗期间,缺少肠道菌群时,虾青素不能改善骨骼肌纤维面积的减少。然而,粪菌移植成功缓解了伪无菌荷瘤小鼠中骨骼肌纤维横截面积的减少(图1D和图2,P < 0.05)。这意味着虾青素膳食补充对靶向治疗荷瘤小鼠的骨骼肌萎缩的有益影响取决于肠道菌群。
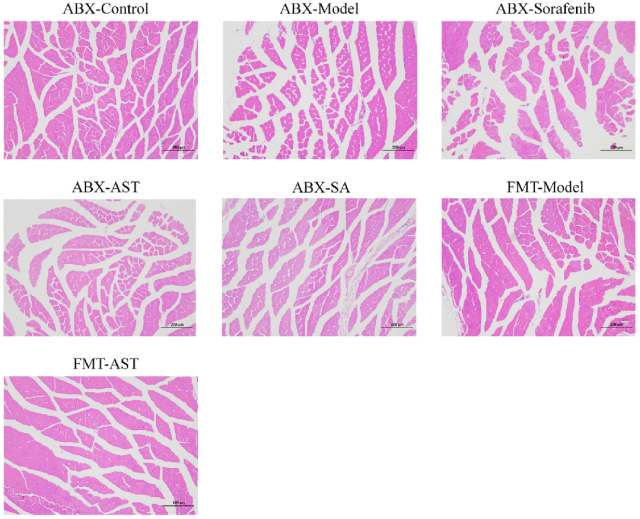
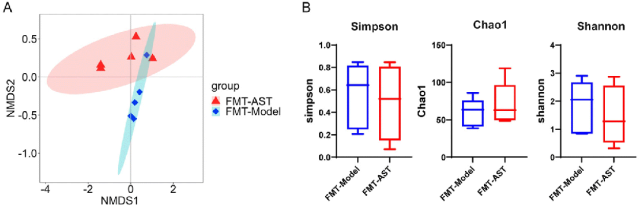
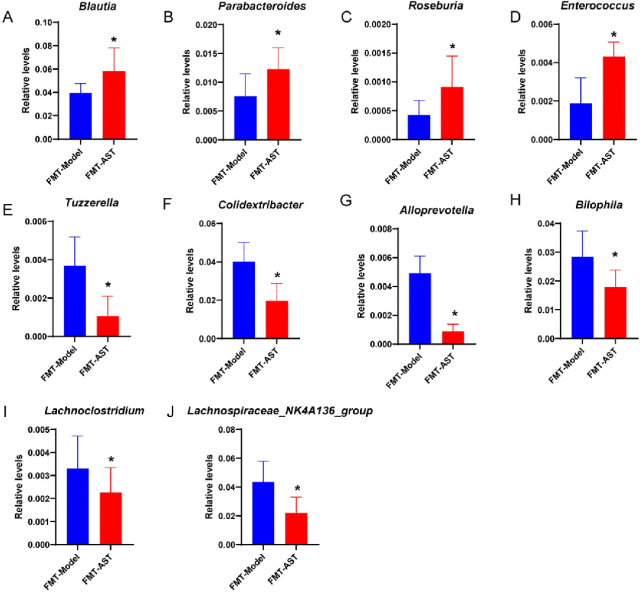
荷瘤小鼠靶向治疗期间,虾青素缓解骨骼肌萎缩的效果依赖于肠道菌群的存在。16s RNA用于分析粪菌移植小鼠的肠道菌群组成,结果见图3。FMT-Model组和FMT-AST组的小鼠表现出不同的肠道菌群组成,表明虾青素膳食补充影响了小鼠肠道菌群组成(图3A)。FMT-Model组和FMT-AST组的肠道菌群α-多样性无明显差异(图3B)。FMT-Model组和FMT-AST组在属水平的物种差异比较分析结果见图4和图S3。与FMT-Model组相比,FMT-AST组的布劳特氏菌属、副杆菌属、罗斯氏菌属和肠球菌的丰度明显更高。在FMT-Model组中,Tuzzerella、Colidextribacteria、嗜胆菌、拟普雷沃氏菌、梭状芽孢杆菌属和毛螺菌属_NK4A136组的丰度更高。这意味着虾青素通过调节肠道菌群组成,缓解分子靶向治疗荷瘤小鼠的骨骼肌萎缩。
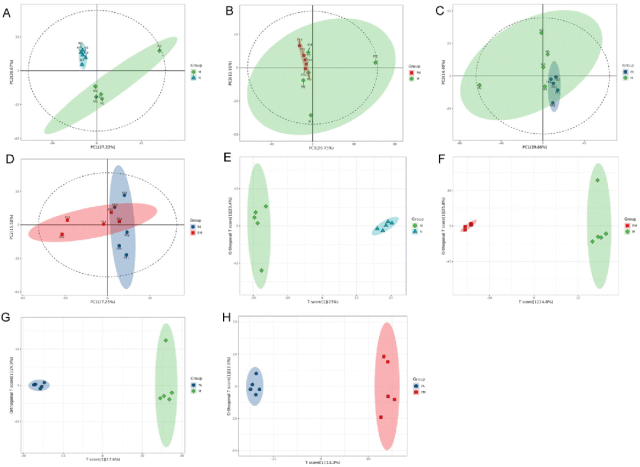
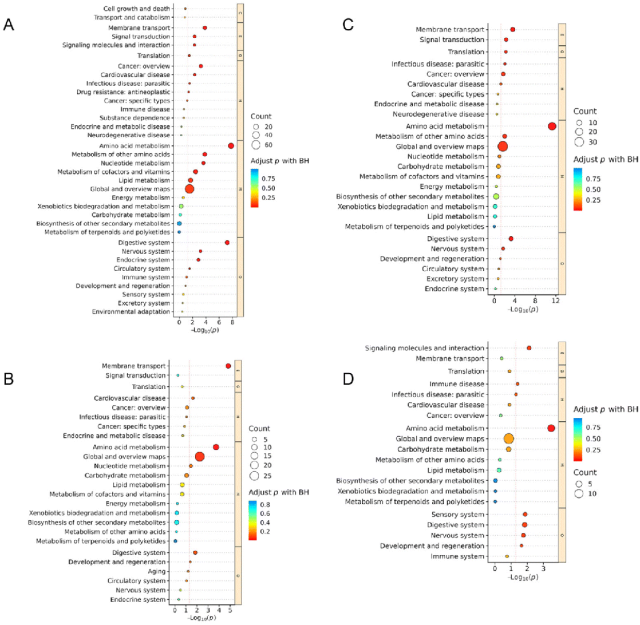
肠道菌群通过微生物的代谢活动影响宿主健康,进而改变生物体外周循环中的代谢物水平。非靶向代谢组学用于分析小鼠血清代谢物的变化。PCA(主成分分析)和OPLS-DA(正交偏最小二乘法判别分析)表明,肿瘤小鼠和无肿瘤小鼠的血清代谢物组成存在显著差异。这些发现表明,肿瘤对机体的代谢过程有重要影响。通过OPLS-DA分析,我们在肿瘤小鼠和无肿瘤小鼠的血清中发现了336种差异代谢物(图5A、E和图S4A)。作者基于京都基因和基因组百科全书(KEGG)分析了差异代谢物的潜在富集途径。肿瘤小鼠和无肿瘤小鼠血清中的差异代谢物主要与氨基酸代谢通路有关,包括赖氨酸降解、色氨酸代谢以及缬氨酸、亮氨酸和异亮氨酸的降解(图6A和图S5A)。这表明,氨基酸代谢异常是恶性肿瘤中骨骼肌萎缩的重要原因。现有文献表明,癌症恶病质与骨骼肌氨基酸和循环氨基酸浓度的变化有关。
粪菌移植对肿瘤小鼠血清代谢物组成有显著影响(图5B、C、F、G和图S4B、C)。具体而言,FMT-Model和FMT-AST组之间的血清代谢物组成存在明显差异(图5B、C和F、G)。这表明虾青素膳食补充通过影响小鼠的肠道菌群对其血清代谢物组成产生了显著影响。FMT-Model组与ABX-Model组之间共鉴定出148种差异代谢物(图5B、F和图S4B)。差异代谢物富集分析表明,这些代谢物主要参与氨基酸代谢途径,包括ABC转运体和赖氨酸降解。FMT-AST组与ABX-Model组之间共鉴定出208种差异代谢物(图5C、G和图S4C)。这些代谢物主要富集在氨基酸代谢途径中,特别是精氨酸生物合成、色氨酸代谢以及缬氨酸、亮氨酸和异亮氨酸生物合成。FMT-AST组与FMT-Model组之间共鉴定出107种代谢物(图5D、H和图S4D)。这些代谢物主要富集在氨基酸代谢途径中,包括组氨酸代谢、色氨酸代谢以及甘氨酸、丝氨酸和苏氨酸代谢。血清代谢组学结果表明,虾青素通过调节肠道菌群和恢复肿瘤发展过程中异常的氨基酸代谢,缓解索拉菲尼诱导的小鼠骨骼肌萎缩。
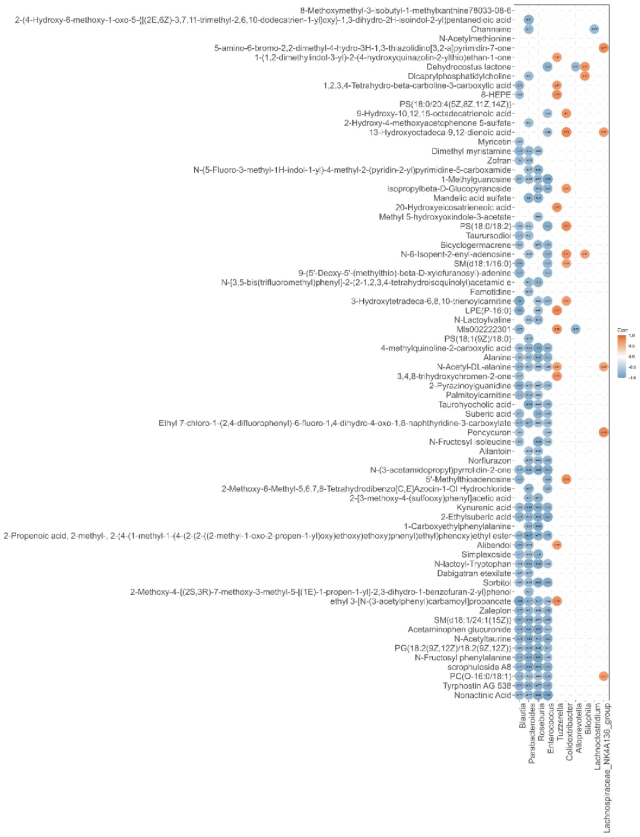
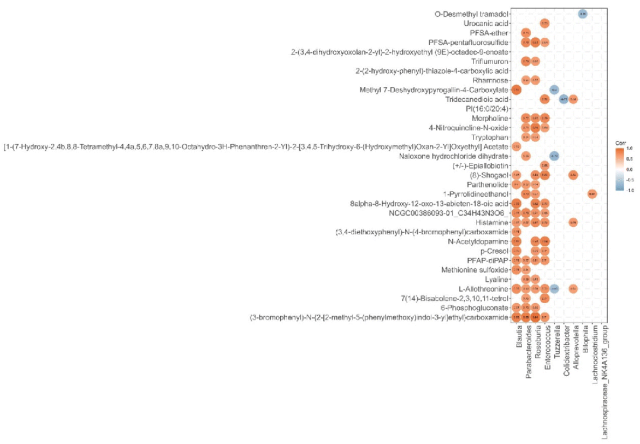
为了更好理解肠道微生物改变与血清代谢物之间的重要关联,作者对FMT-Model和FMT-AST中观察到的10种差异菌与血清中的107种显著差异代谢物进行相关性分析。图7为FMT-AST中差异下调代谢物与肠道微生物之间的相关性分析热图。在FMT-AST中显著下调的差异代谢物与FMT-AST中显著增加的微生物(如布劳特氏菌属、副杆菌属和罗斯氏菌属)之间存在明显的负相关。图8显示的热图为FMT-AST中上调的差异代谢物与肠道微生物之间的相关性分析结果。在FMT-AST中显著上调的差异代谢物与在FMT-AST中显著增加的微生物(如布劳特氏菌属、副杆菌属和罗斯氏菌属)之间存在明显的正相关。这些结果表明,布劳特氏菌属、副杆菌属、罗斯氏菌属和肠球菌的变化可能在调节血清代谢物中发挥重要作用。
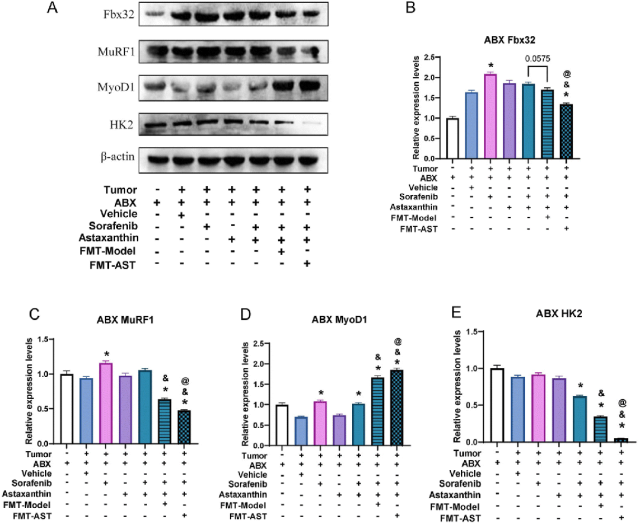
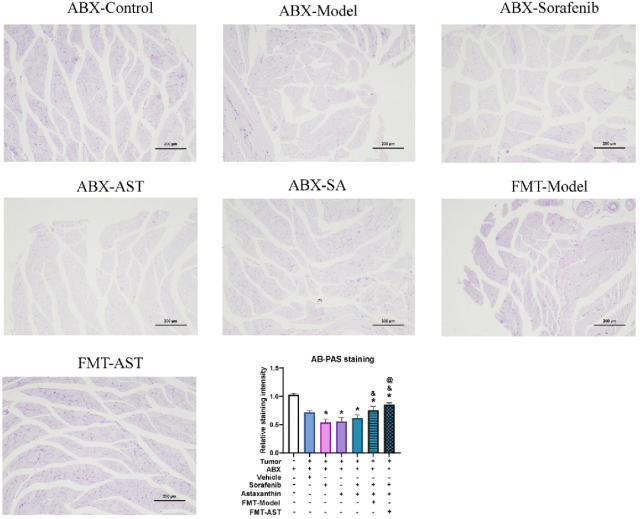
氨基酸是肌肉蛋白质的重要组成部分。氨基酸代谢异常会破坏蛋白质合成与分解,导致骨骼肌营养供应不足,进而引起肌肉萎缩。作者评估了荷瘤小鼠骨骼肌中参与蛋白质降解和合成的关键成分的蛋白质表达。Fbx32和MuRF1作为骨骼肌蛋白质降解的主要调节因子,被认为是骨骼肌萎缩的重要生物标志物。蛋白免疫印迹分析显示,与无肿瘤小鼠相比,Fbx32在荷瘤小鼠骨骼肌中的表达明显升高(图9A-C,P < 0.05)。此外,索拉菲尼进一步增加了Fbx32和MuRF1的水平(图9A-C,P < 0.05)。这些发现表明,索拉菲尼治疗会加剧骨骼肌萎缩,肌肉质量及其横截面积的检测结果也证明了这一点。然而,在缺少肠道菌群情况下,虾青素对Fbx32和MuRF1没有抑制作用(图9A-C,P < 0.05)。相反,粪菌移植有效恢复了虾青素对Fbx32和MuRF1表达的抑制作用,从而减少骨骼肌萎缩。MyoD1是参与调节骨骼肌发育和分化的重要转录因子。此外,本研究还发现粪菌移植增强了虾青素促进MyoD1表达的能力(图9D,P < 0.05)。肌糖原可在肌肉降解过程中补充骨骼肌的能量储备,从而为肌肉功能提供支持。本研究利用AB-PAS(阿尔新蓝/过碘酸雪夫)染色法分析骨骼肌中的肌糖原含量。结果见图10。肿瘤明显降低了骨骼肌中的糖原染色强度。在清除荷瘤小鼠的肠道菌群之后,服用虾青素没有使骨骼肌中糖原水平增加。然而,粪菌移植有效恢复了虾青素增强肌糖原储存的能力。研究发现,在索拉菲尼和虾青素联合治疗的小鼠中,FMT显著降低了其骨骼肌HK2(一种参与糖原分解的重要代谢酶)的表达(图9E,P < 0.05)。FMT-AST的效果显著优于FMT-Model。这些研究结果表明,虾青素具有潜在延缓分子靶向治疗荷瘤小鼠骨骼肌萎缩的能力,防止其肌糖原降解的作用。这一作用通过调节肠道菌群实现。
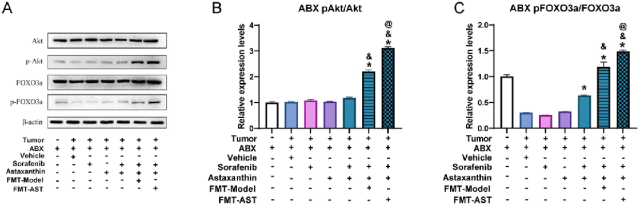
Akt/Foxo3a信号轴在控制骨骼肌萎缩和肌生成中起着关键作用。小鼠体内的肿瘤导致p-Foxo3a/Foxo3a水平显著下降。此外,与ABX-SA组和ABX-Model组相比,FMT-Model组和FMT-AST组小鼠的p-Akt/Akt和p-Foxo3a/Foxo3a水平均显著升高(图11,P < 0.05)。与FMT-Model组相比,FMT-AST组的p-Akt/Akt和p-Foxo3a/Foxo3a水平明显升高(图11,P <0.05)。这表明虾青素通过影响肠道菌群的代谢活动来影响Akt/Foxo3a信号通路,从而减缓骨骼肌萎缩。
讨论
在之前的研究中,作者发现在接受索拉菲尼治疗的H22小鼠的饮食中添加虾青素有效改善了骨骼肌萎缩和体重减轻。此外,虾青素显著影响了H22小鼠肠道菌群的组成。最近的研究表明,肠道菌群对维持机体的生理平衡至关重要。因此,作者猜想虾青素主要作用于肠道菌群,以缓解癌症相关恶病质的骨骼肌萎缩。即使通过抗生素消除了肠道菌群,荷瘤小鼠的体重减轻和骨骼肌萎缩依然存在,这表明体内的肿瘤对引起骨骼肌萎缩有重要作用。尽管观察到索拉菲尼治疗能减缓肿瘤发展,但它未能有效缓解骨骼肌萎缩,事实上,它似乎加重了骨骼肌萎缩(图S2)。与之前缓解骨骼肌萎缩方法的效果不同,虾青素在伪无菌荷瘤小鼠中的疗效有限。粪菌移植有效改善了ABX-SA小鼠的骨骼肌萎缩,且Donor-AST小鼠的粪菌移植效果优于Donor-Model小鼠。这些结果表明,虾青素可能主要作用于肠道菌群,以改善索拉菲尼治疗期间的骨骼肌萎缩。并且,虾青素缓解骨骼肌萎缩的能力似乎取决于健康肠道菌群是否存在。此外,阐明虾青素对调节肠道菌群的影响十分重要。作者对粪菌移植的小鼠肠道菌群组成进行分析。研究结果表明,FMT-AST组和FMT-Model组小鼠的菌群组成和结构存在明显差异。这项研究为虾青素通过调节小鼠肠道菌群缓解骨骼肌萎缩提供了更多证据。肠道菌群的α-多样性在FMT-AST组和FMT-Model组之间没有显著差异。这一发现表明虾青素并不能通过恢复伪无菌小鼠的肠道菌群结构发挥作用。相反,肠道菌群中优势物种发生变化。作者随后对两组小鼠的主要差异微生物进行分析。属水平上,鉴定出10种差异微生物,其中,在FMT-AST组中,4种表现出显著上调,6种表现出显著下调。粪便移植后小鼠肠道菌群中的差异微生物与作者之前实验中观察到的微生物相似。这些结果表明,这些细菌可能是虾青素靶向调节的关键菌属。此外,作者还确定了这些差异微生物和小鼠粪菌移植后血清中显著变化的代谢物之间的相关性。研究发现,FMT-AST中微生物的增加与血清中差异代谢物之间存在明显的相关性。这意味着布劳特氏菌属、副杆菌属、罗斯氏菌属和肠球菌水平的改变或许可解释血清代谢的变化。近年来,布劳特氏菌属作为一种潜在提高宿主代谢健康的下一代益生菌而倍受关注。副杆菌属是肠道中普遍存在的共生菌。罗斯氏菌属被认为是肠道中主要的丁酸产生菌,也被认为是一种潜在的下一代益生菌。这些发现为虾青素调节肠道菌群组成的潜能提供了更多证据。
肠道微生物的代谢活动影响宿主外周循环中代谢物水平的变化。非靶向代谢组学研究表明,氨基酸代谢在肿瘤诱导的骨骼肌萎缩中起着重要作用。本研究中,与无肿瘤的正常小鼠相比,小鼠体内肿瘤导致氨基酸代谢异常。与正常生物体相比,癌症恶病质的氨基酸代谢过程明显异常。氨基酸是蛋白质的基本成分,对肌肉的合成和维持具有重要作用。与正常组织细胞相比,肿瘤组织的蛋白质分解代谢加快,蛋白质合成减少。此外,肿瘤组织可能从正常组织中捕获蛋白质产物来合成肿瘤生长所必需的蛋白质。这最终会导致体内氨基酸的严重过度消耗。肠道菌群通过分解食物为人体提供必需氨基酸,并影响氨基酸的生物利用度。例如,微生物的赖氨酸产量极大地满足了啮齿动物和猪对氨基酸的需求。研究表明,小鼠肠道乳酸菌水平的提高可引起粪便氨基酸组成的重大改变。补充副干酪乳杆菌NCC2461菌株与啮齿动物粪便中氨基酸模式的变化有关。肠道菌群对食物氨基酸的分解代谢会导致宿主氨基酸的净损失。并且,肠道菌群还能影响肌肉细胞中蛋白质的分解、生成和调节,进而通过调节氨基酸代谢来防止骨骼肌退化。此外,一些研究发现,提升肠道菌群稳态可以增强癌症患者骨骼肌的力量和功能。这些结果表明,肠道菌群与骨骼肌萎缩的产生和发展有重要关系。Donor-AST的粪菌移植至无菌荷瘤小鼠对氨基酸代谢的调节产生影响,并减缓了肌肉萎缩。这表明虾青素可能通过调节肠道菌群改变荷瘤小鼠的氨基酸代谢,进而减缓肿瘤诱发的骨骼肌萎缩。
此外,虾青素还可能通过影响肠道菌群调节骨骼肌的葡萄糖代谢,从而减轻肿瘤引起的骨骼肌萎缩。肿瘤的发展会导致体内能量利用效率低下。研究表明,在癌症病例中,骨骼肌利用葡萄糖的主要模式是无氧糖酵解,而不是氧化磷酸化。由于肿瘤细胞对能量的需求增加,骨骼肌必须进行糖酵解以产生乳酸,乳酸随后被输送至肝脏,在肝脏中通过糖异生转化为葡萄糖。骨骼肌中肌糖原水平的降低是无氧糖酵解增加的另一个直接后果。前人研究表明,糖酵解抑制剂2-脱氧-D-葡萄糖可通过抑制骨骼肌中HK2的活性,减缓癌症恶病质相关的骨骼肌萎缩。本研究中,粪菌移植后的荷瘤小鼠骨骼肌中肌糖原水平显著增加,糖酵解相关酶HK2的表达显著下降。这表明肿瘤小鼠利用骨骼肌分解代谢为机体提供能量的程度降低,从而阻止骨骼肌萎缩。此外,虾青素减缓骨骼肌糖酵解的作用机制可能肌细胞线粒体功能的修复有关。线粒体是骨骼肌氧化磷酸化的主要场所,线粒体功能受损常被发现于癌症恶病质导致的骨骼肌萎缩中。修复线粒体功能障碍有助于提高能量产生的效率,减缓骨骼肌中糖酵解的速度。无菌小鼠骨骼肌的线粒体DNA含量和线粒体生物合成基因的表达水平均有所降低。然而,在移植了正常小鼠的肠道菌群后,这些不足得到明显改善。最近的研究表明,线粒体功能障碍也影响恶病质骨骼肌的氨基酸代谢,这似乎是由CAT1表达减少以及线粒体蛋白降解引发的。接受粪菌移植的伪无菌荷瘤小鼠的氨基酸代谢发生显著改变,这表明骨骼肌中的线粒体功能被修复。这些结果表明,虾青素通过调节肠道菌群在改善恶性骨骼肌萎缩方面发挥着关键作用。然而,确定骨骼肌中的糖酵解和氧化磷酸化调节如何被调节,以及肠道菌群如何影响骨骼肌中的糖酵解,还需要进一步的研究。
PI3K/AKT通路对肌肉组织中蛋白质合成至关重要。它的激活不仅阻碍重症肌无力相关蛋白的转录,而且阻止肌纤维蛋白的降解。研究表明,阻断这一途径导致蛋白质合成减少,蛋白质水解增加。此外,AKT会抑制FoxO3蛋白的磷酸化,进而抑制由这些蛋白调控的自噬激活,促进肌肉萎缩。对AKT/FoxO3a信号通路的研究证实,虾青素通过肠道菌群影响氨基酸代谢,减缓了荷瘤小鼠骨骼肌萎缩的进程。肌肉特异性E3泛素连接酶Atrogin1和MuRF1与肿瘤恶性中肌肉萎缩的关系已被广泛研究。这些蛋白被广泛认为是肌肉萎缩的关键标志物,负责选择性泛素化目标蛋白的降解。在移植Donor-AST小鼠的盲肠细菌后,伪无菌小鼠的骨骼肌中MuRF1和Fbx32的表达水平显著下降,MyoD1的表达水平显著上升,表明肿瘤引起的骨骼肌蛋白降解和合成异常被恢复。这表明虾青素通过特异性靶向肠道菌群影响氨基酸代谢,而肠道菌群在骨骼肌萎缩的发展过程中起着至关重要的作用。
本研究表明,虾青素可通过调节肠道菌群有效缓解荷瘤小鼠的骨骼肌萎缩和体重减轻。肿瘤患者易出现骨骼肌萎缩和体重减轻,从而导致恶病质。治疗肿瘤的难度由此加大,最终患者的存活率降低。膳食中补充虾青素有可能改善骨骼肌萎缩,但这依赖于肠道菌群促进这一过程的能力。这些发现对肿瘤患者的膳食补充配方和虾青素资源的优化利用具有重要意义。
结论
肠道微生物的存在影响虾青素减轻治疗期中荷瘤小鼠骨骼肌萎缩的效果。虾青素通过调节肠道菌群组成影响血清代谢物水平,特别是通过促进布劳特氏菌属、副杆菌属、罗斯氏菌属和肠球菌属的生长。虾青素显著调节了荷瘤小鼠的氨基酸代谢,减缓骨骼肌蛋白质的泛素化分解,促进蛋白质合成。此外,研究结果还表明,虾青素可通过Akt/Foxo3a信号通路阻碍H22荷瘤小鼠的骨骼肌萎缩。这些发现为将虾青素作为肿瘤患者的膳食补充剂奠定了理论基础。
